Data:2020年10月22日 Click:0 Release:1
引言
糖尿病是21世纪发展最快的健康问题之一,根据国际糖尿病联盟(IDF)的保守统计,2019年全球20-79岁的成年人有约4.63亿患有糖尿病,按照目前的增长速度,到2030年成人糖尿病患者将达到5.78亿,2045年达到7亿【1】。糖尿病的流行正在给全球医疗带来严峻的挑战。目前糖尿病药物共有8类,在这8类药物中,胰高血糖素样肽(GLP-1)类药物凭借除降糖外兼具心血管获益和减重效果,得到了各大糖尿病治疗指南的强力推荐。GLP-1类药物市场发展迅速,2018年市场规模就已达到了93亿美元,增长率高达25%【2】。然而,相比目前的波涛汹涌,早期GLP-1类药物市场则要风平浪静得多,一个重要的原因便是作为多肽的GLP-1体内半衰期短,需要频繁注射给药,患者依从性差。纵观GLP-1类药物的研发历程(附图1)几乎都离不开半衰期的延长,事实上这也代表了蛋白质多肽类药物的普遍趋势。本文将对已上市的GLP-1类药物的长效化进行回顾,以期为本领域的药物研发提供有益借鉴。
艾塞那肽
20世纪70至80年代,全世界掀起了一股研究新型肽激素肽的热潮。在这样的时代背景下,1977年诺贝尔生理学奖得主罗莎琳·萨斯曼·耶洛负责的实验室致力于在不同动物体内寻找新的激素,在此期间,约翰·恩博士在希拉毒蜥(Gila monster)的毒液中找到了一种新的多肽,并将其命名为Exendin-4,这便是如今的艾塞那肽【3】。艾塞那肽的氨基酸序列和人体内的GLP-1约有53%的相似性,其活性甚至强于GLP-1,更为重要的是相比于GLP-1的不足2min,艾塞那肽在人体内的半衰期达到了2.4小时,成药性更大。于是,在2005年,Exendin-4发现的第13年,经历了一番曲折之后FDA批准了艾塞那肽注射液(Byetta®)的上市申请,用于服用口服降糖药无法控制的2型糖尿病患者的血糖辅助控制。随后,为了进一步延长艾塞那肽的作用效果,阿米林(Amylin)和礼来(Eli Lilly)公司开发了艾塞那肽注射微球(Bydureon®),该药物于2012年1月在美国获得了批准。和每天注射两次的Byetta相比,Bydureon只需每周注射一次。作为第一个上市的GLP-1周制剂,Bydureon极大地提高了患者的依从性,GLP-1长效制剂的优势开始显现【3】。
向自然界学习,是人们在长期的生产实践中总结出来的经验,艾塞那肽的发现便是很好的例子。作为第一个成功上市的GLP-1类药物,艾塞那肽为之后的药物研究提供了极好的模板。人体内GLP-1之所以降解迅速,很大程度上是因为第8位的丙氨酸容易被二肽基肽酶(DPP-4)识别并切割,艾塞那肽该位置为甘氨酸,很好地抵抗了DPP-4降解。受此启发,后来上市的利司那肽、聚乙二醇洛塞那肽均是在艾塞那肽的基础上进行氨基酸替换和修饰,阿必鲁肽、度拉糖肽虽然用的是人GLP-1,但序列上该位置也都改为了甘氨酸。
利拉鲁肽和索马鲁肽
2010年1月25日,FDA批准了诺和诺德公司利拉鲁肽注射液(Victoza ®)的上市申请,如果说艾塞那肽是另辟蹊径,利拉鲁肽则是对GLP-1体内易降解这一难题的正面回应。
脂肪酸是构成细胞膜磷脂及人体脂肪与类脂的重要成分,直接参与了细胞膜的组成以及蛋白质配体与膜受体的结合,脂肪酸修饰有助于提高药物脂溶性、肠道粘膜透过性及吸收效率。而且,引入脂肪酸可以增加药物的疏水性,掩盖蛋白水解酶结合位点。另外,最令人感兴趣的是脂肪酸能够和血清白蛋白(HSA)可逆结合。HSA是人体血浆中含量最丰富、结构最稳定的蛋白质,半衰期长达数周。药物通过脂肪酸侧链同HSA结合后,流体力学半径和分子量增加,肾小球过滤减少,体内滞留时间大大延长【4,5】。
1998年,第一篇以GLP-1为研究对象,描述脂肪酸侧链作为药物同HSA连接桥梁的论文发表,作者是来自糖尿病巨头礼来公司的研究者。而早在1994年,另一糖尿病巨头诺和诺德(Novo Nordisk)就已将目光瞄准了GLP-1的脂肪酸侧链修饰。彼时,诺和诺德刚经历了GLP-1缓释制剂开发的失败,礼来和罗氏(Roche)也经受了相同遭遇。这一困境促使诺和诺德的研究者们转变思路。通过丙氨酸扫描,他们细致地考察了GLP-1序列中每个氨基酸的重要性,并设计了一系列具有抵抗DPP-4酶降解的类似物,然而,这些类似物的半衰期并不能满足每天给药1次的要求。恰巧此时,脂肪酸侧链修饰胰岛素(地特胰岛素)项目取得了不错的进展,对GLP-1改造结果感到不满意的研究者们于是决定使用脂肪酸侧链。为了达成利拉鲁肽项目之初设定的4个目标:(1)受体效价小于500 pM;(2)半衰期超过10h;(3)代谢稳定性强于天然GLP-1,能够抵抗DPP-4和其他蛋白酶的降解;(4)尽可能地接近人体GLP-1序列,以避免产生免疫原性,年轻的研究者们首先克服了脂肪酸侧链修饰产物纯化的难题,经过一遍又一遍的筛选,终于从近40个候选物中获得了利拉鲁肽【6-8】。
利拉鲁肽氨基酸序列上和天然GLP-1仅相差第34位一个氨基酸(K34R,避免发生侧链的非特异性连接),第26位赖氨酸通过γ-谷氨酸接头同16烷酸相连(附图2),可通过微生物重组表达和简单化学反应获得。为了保证受体效价,利拉鲁肽并没有将第8位丙氨酸改为甘氨酸,但是得益于脂肪酸侧链修饰,利拉鲁肽的半衰期达到了13h。和艾塞那肽相比利拉鲁肽降糖效果更强,且每天只需注射一次,患者依从性更高,而其后的研究更是证明利拉鲁肽具有减肥效果。上市后利拉鲁肽的销售额很快便超过了艾塞那肽,成为GLP-1受体激动剂领域第一个重磅药物。
利拉鲁肽获得成功后,面对GLP-1市场的云谲波诡,诺和诺德并没有停止探索的脚步。为了进一步延长GLP-1的半衰期,需要强化GLP-1药物分子同HSA结合的紧密程度,而大量的研究表明,HSA会阻碍GLP-1分子和受体的结合,造成效价下降。因此,新的药物分子必需同时具有较高的HSA结合力以及受体亲和力,诺和诺德沿袭了利拉鲁肽的设计思路,尽量保证多肽序列和天然GLP-1一致,同时把研究的重点放在脂肪酸侧链的选择上。在利拉鲁肽的基础上,再次筛选了40余个候选物,最终得到了索马鲁肽。和利拉鲁肽相比,索马鲁肽将第8位丙氨酸替换成了γ-氨基异丁酸(Aib),Aib在之前的研究中已经被证明在抵抗DPP-4降解的同时,不会对GLP-1的受体亲和力造成不利影响。另外,索马鲁肽的侧链结构也更为复杂(附图2)。这些改变赋予了索马鲁肽长达约160h的半衰期,用于控糖每周只需注射一次。索马鲁肽注射液Ozempic ®于2017年12月16日获得了FDA批准,凭借降糖和减重方面等方面的优势,成为了有史以来最好的GLP-1类药物【6-8】。
度拉糖肽和阿必鲁肽
作为诺和诺德糖尿病领域长期以来的对手,眼见利拉鲁肽大获成功,礼来自然不会冷眼旁观。对于GLP-1的脂肪酸侧链修饰,礼来虽然早期也曾做过尝试【6】,却并没有在该领域有所建树,反倒是选择的另外一条长效化路线——Fc融合蛋白促成了度拉糖肽的诞生。
Fc融合蛋白技术是目前研究最多、进展最快的蛋白融合技术。受体介导的细胞内吞、溶酶体降解作用是蛋白清除的重要途径,而在血浆中,免疫球蛋白IgG相对分子质量大于肾脏过滤阈值。并且,利用保守区Fc片段和新生儿Fc受体(FcRn)识别,通过FcRn介导的再循环机制,IgG可以逃避细胞内吞后的溶酶体降解,半衰期可达2至3周【4,5】;度拉糖肽正是利用Fc片段的这一特性,通过16氨基酸接头将氨基酸替换后的GLP-1分子连接至Fc片段的N端(附图3),以此来延长半衰期。度拉糖肽的半衰期达到了90h,研究表明其每周注射一次的降糖效果不劣于每日注射一次利拉鲁肽【9,10】。自上市以来,度拉糖肽销售额每年都保持着高速增长,2019年针对糖尿病适应症已超过利拉鲁肽,如果不是后面上市的索马鲁肽,礼来将在GLP-1领域扳回一城。
2014年FDA批准了首个HSA融合蛋白药物阿必鲁肽(Tanzeum®)。同利拉鲁肽以及索玛鲁肽一样,阿必鲁肽也是借由HSA来实现长效目的,不同之处在于,利拉鲁肽和索玛鲁肽通过脂肪酸和HSA的结合是可逆的,GLP-1药物分子可以脱离HSA发挥作用,而阿必鲁肽则是通过基因工程手段将串联重复的两个GLP-1分子和HSA融合表达成为一个新的蛋白分子,这种融合的方式和度拉糖肽相似。串联重复的目的在于使GLP-1分子N端远离HSA,以减少HSA对受体结合的干扰,另外,为了抵抗DPP-4的降解,阿必鲁肽中GLP-1分子第8位丙氨酸被替换成了甘氨酸【11】。作为同年上市的两种GLP-1周制剂,阿必鲁肽的半衰期甚至长于度拉糖肽,但是由于其降糖效果不及利拉鲁肽,上市后反响平平。然而,换个角度,作为首个FDA批准的HSA融合蛋白,阿必鲁肽无疑为HSA融合蛋白药物的研发提供了很好的范例,除原研企业GSK外,其他企业如CSL、Teva也纷纷开展了HSA融合蛋白的研究。
聚乙二醇洛塞那肽
2016年12月19日,国家药品监督管理局(NMPA)批准了贝那鲁肽的上市申请。贝那鲁肽号称全球首个氨基酸序列与人源完全一致的GLP-1类药物、第一个国产GLP-1类药物【12】。然而,正是由于序列全人源化,贝那鲁肽体内半衰期极短,每天3次的注射频率饱受病人诟病。作为我国第一个原研完全拥有自主知识产权的GLP-1制剂,贝那鲁肽试图打破国外厂家在该领域的垄断似乎显得心有余而力不足。好在2019年5月,另一个国产GLP-1类药物聚乙二醇洛塞那肽上市,有效地缓解了这一尴尬局面。
聚乙二醇(PEG)是FDA批准的极少数能作为体内注射药用的合成聚合物之一,具有较低的相对分子质量多分散性、良好的水相和有机可溶性,在蛋白药物的修饰中应用十分广泛。PEG可将球形修饰蛋白的表观相对分子质量提高5至10倍,显著减少蛋白药物的肾小球过滤。此外,PEG化可降低网状内皮组织对蛋白药物的清除、屏蔽抗原决定簇,降低免疫系统识别作用、阻止蛋白水解酶的降解【4,5】。聚乙二醇洛塞那肽是由江苏豪森药业自主研发的1类化药,用药上只需每周注射1次。药物分子上,聚乙二醇洛塞那肽选择了艾塞那肽,不同的是第8位突变为D-Ala,另外以赖氨酸为接头,在半胱氨酸位点将其聚乙二醇化(附图4)【13】。作为第一个国产长效GLP-1受体激动剂,聚乙二醇洛塞那肽从初次申报临床到获批经历了十余年时间,后续表现如何,让我们拭目以待。
结语
GLP-1类药物是蛋白质多肽类药物的一个分支,它的发展代表了蛋白质多肽药物从短效到长效的整体趋势。GLP-1的长效化策略并不是量身打造,文中所述GLP-1类药物的长效化策略(氨基酸替换、脂肪酸侧链修饰、Fc融合蛋白、PEG化)只是目前长效化策略的一个小部分,实际上这些策略早在其他蛋白质多肽药物上就有应用。反过来,这些在GLP-1上获得成功的长效化策略也为其他药物提供了良好的范例。
鉴于现有GLP-1类药物尤其是索马鲁肽的突出表现,代谢类疾病如糖尿病领域的药物研发已经进入了多靶点时代。尽管新的长效化方法不断涌现,但目前在研的大部分药物其长效方式依然沿用了单靶药物。对于企业而言,如果建立了强大的长效化平台,药物推陈出新的速度将会大大加快,比如诺和诺德,其研发的地特胰岛素、德谷胰岛素、利拉鲁肽、索玛鲁肽都是基于脂肪酸侧链修饰,可谓一招鲜吃遍天。国内一些药企也正在建立自己的平台,如鸿运华宁将GLP-1和抗体偶联,药物半衰期无疑会进一步延长。
GLP-1从发现至今已经走过了35个年头,已不再是新靶点,但其长效化的道路却还远没有结束!
附表和附图
附表已上市GLP-1类药物的长效化策略及药物半衰期
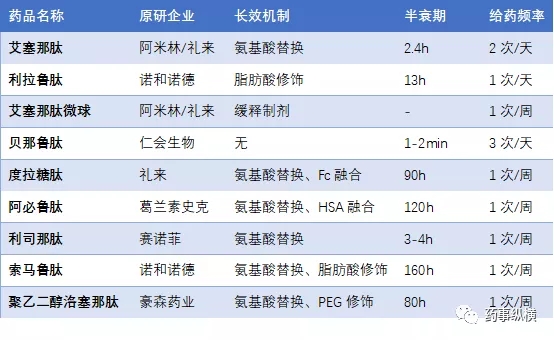
附图1 GLP-1类药物的研发历程
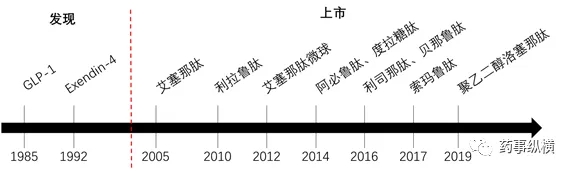
附图2 利拉鲁肽(Liraglutide)和索马鲁肽(Semaglutide)【8】
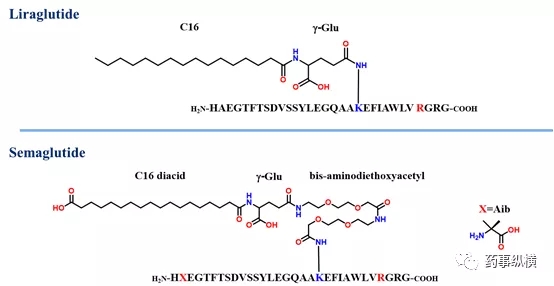
附图3 度拉糖肽【10】
附图4 聚乙二醇洛塞那肽【13】

参考资料:
【1】IDF全球糖尿病概览2019年第9版宣传指南
【2】医药经济报:GLP-1药物迎来“搅局者”. http://www.yyjjb.com.cn/
【3】药事纵横:GLP-1的发现故事——从艾塞那肽说起. https://mp.weixin.qq.com/s/OdC2PbwKu8DoknY5K002bw
【4】杜昭明,徐寒梅,王轶博等.长效蛋白多肽类药物技术研究进展[J]. 药物生物技术,2017, 024(001):63-67.
【5】梁成罡, 王军志. 长效蛋白生物药研究进展[J]. 中国新药杂志, 2014(20).
【6】Knudsen LB. Inventing Liraglutide, a Glucagon-Like Peptide Analogue, for the Treatmentof Diabetes and Obesity[J]. Acs Pharmacology & Translational Science, 2019,2(6):468-484.
【7】Lotte, Bjerre, Knudsen, et al. TheDiscovery and Development of Liraglutide and Semaglutide.[J]. Frontiers inendocrinology, 2019, 10: 155.
【8】Lau J ,Bloch P , Lauge Schäffer, et al. Discovery of the Once-Weekly Glucagon-LikePeptide-1 (GLP-1) Analogue Semaglutide[J]. Journal of Medicinal Chemistry,2015, 58(18):7370.
【9】Kathleen, M Dungan, et al.Once-weeklydulaglutide versus once-daily liraglutide in metformin-treated patients withtype 2 diabetes( AWARD-6) : a randomised,open-label,phase3, non-inferiority trial [J].Lancet,2014,384 ( 9951) : 1349 - 1357.,
【10】Naver S, Jimenez-Solem E, Christensen M, et al.Dulaglutide: a novel once-weekly glucagon-like peptide-1 receptor agonist[J].Clinical Investigation, 2014, 4(8): 729-743.
【11】T.D. Müller, Finan B ,Bloom S R , et al. Glucagon-like peptide 1 (GLP-1)[J]. Molecular Metabolism,2019, 30.
【12】上海仁会生物官网.http://www.benemae.com/
【13】制药在线:聚乙二醇洛塞那肽!国产长效GLP-1R激动剂. https://m.cphi.cn/news/show-167652.html
来源:药事纵横


